把猪器官移植到猕猴甚至人体内,听起来是天方夜谭,但作为5年前“冷启动”的热土,异种器官移植在2025年取得的突破,比过去100年都多。
一枚基因编辑猪肾,在美国大叔蒂姆·安德鲁斯(Tim Andrews)的体内正常工作了近九个月,刷新了全球猪肾移植患者的存活纪录。但在10月23日,因为移植肾功能衰退,这枚猪肾被摘除,安德鲁斯重新恢复透析,纪录也定格在271天。
不过,华中科技大学同济医学院附属同济医院器官移植外科主任医师、长江学者特聘教授、国内器官移植领域权威专家陈忠华,却从历史长河中翻出一个有趣的案例:1964年,一位美国女教师接受黑猩猩肾脏移植后,存活了近9个月(269天),仅比此次美国猪肾移植患者创下的最新存活纪录(271天)少两天。
也就是说,经过60多年的努力,异种器官移植到人类体内的存活纪录仅提高了两天。对比人工心脏取得的实质性进步,异种器官移植所做的努力是否还远远不够?
“绝对不是。”近日,陈忠华接受《每日经济新闻》记者(以下简称NBD)专访时表示:“我们不会把它(指全球猪肾移植最长纪录保持者摘除猪肾)定义为失败,而是一个新的里程碑。”
2天之差的本质:基因编辑与免疫抑制的60年跃迁有报道称,安德鲁斯的案例,打破了此前由阿拉巴马州一名女性保持的130天纪录,为异种移植领域带来新曙光。
但事实上,在安德鲁斯之前,最长存活纪录来自另一位23岁的勇敢女性:1964年1月13日,美国女教师伊迪斯·帕克(Edyth Parker)接受了黑猩猩肾脏移植,手术后曾重返教师岗位工作,最终在移植满9个月的前一天因为心功能失常突然去世,而病理检查发现移植肾基本正常。

异种器官移植临床探索历史图片来源:受访者提供
NBD:这两个案例有哪些不同之处?
陈忠华:两位患者都存活了9个月左右,但背后的差异显著。
第一,上世纪六十年代,免疫抑制方案处于原始阶段,没有特效的免疫抑制剂,其(案例)优势在于黑猩猩与人类的基因差异性比猪小得多,属于协调性异种移植(concordant),免疫兼容性更强;再加上个体差异,美国女教师实现了接近九个月的存活。
第二,当年十几例黑猩猩肾移植患者中,只有这1例存活近9个月,其余均在2个月内失败。而安德鲁斯接受的是基因编辑猪肾移植,即非协调性异种移植(discordant),基因差异比灵长类大得多。再加上现代免疫抑制药物等技术支持,他存活超过了9个月时间。
第三,美国女教师是突然过世,但肾脏功能基本完好;安德鲁斯是摘除了移植器官后仍然存活。这是重要区别。
NBD:当年那位女教师的死亡原因是什么?
陈忠华:经后世分析,很可能是血钾/钙等电解质代谢紊乱导致心功能失常,进而猝死。动物器官移植到人体内,除了免疫排斥反应,还存在生物适配问题。灵长类动物与人类在水盐电解质代谢上仍有不同,但当时的人们尚未重视到电解质代谢紊乱对生命的潜在风险。
而如今,异种器官移植患者主要面临的问题是免疫排斥反应。蒂姆·安德鲁斯在9个月内经历了多次病情反复,医生不断调整免疫抑制方案,让他度过了以分钟、小时或天计算的“超急性排斥反应”,以及3个月到半年的高危险期。
这说明,综合性的药物使用能够基本控制早期的急排斥反应。
NBD:既然黑猩猩比猪的优势明显,为何现在使用猪的器官呢?
陈忠华:主要有三个原因。一是伦理学层面,灵长类动物是人类的近亲,情感与人类高度相似,有些甚至是保护类动物,动物实验以及日后大规模应用的伦理审查很难通过。
二是生物安全风险。亲缘关系越近,人畜共患疾病的可能性越大,灵长类动物体内的内源性逆转录病毒亚型更多,而且无法完全敲除,移植后复活的概率也更高。例如,艾滋病的起源就被认为与黑猩猩相关。
三是实用性。灵长类动物繁殖周期长、数量稀少,无法满足大规模移植需求,经济上也不具备可行性。而猪可以大量繁殖,通过基因编辑技术,可精准修饰关键基因,拉近与人类的免疫兼容性,这是近三十年的重要技术进步。
最近几年,我也重新审视过灵长类动物器官移植的可行性,发现仍不可行。一方面,目前很难对灵长类动物进行基因编辑;另一方面,其基因内携带的内源性逆转录病毒等风险因子无法彻底清除,生物安全性低于猪的器官。
所以,并不是说60多年只进步了2天,其实是已经进入下一轮(猪器官移植)的冲刺阶段了。
直面三大瓶颈:基因编辑、免疫抑制与审批机制之困无论是安德鲁斯,还是接受猪肾移植的中国患者,基本上都患有尿毒症。
这是一种凶险的疾病,患有这种疾病的患者是器官移植的典型适用群体。患者如果不接受透析或肾移植等替代治疗,死亡率接近100%;即使接受规律透析治疗,死亡率仍可达50%~80%。在国内,可用于移植手术的器官供给紧缺,按已经登记的等待者数量计算,2024年国内器官供需比大约是1∶8。
因此,异种器官移植被寄予厚望,但面临的挑战仍然严峻。
陈忠华打了个比方,尿毒症患者就像被狮子追赶的羚羊,要么选择长期透析,要么跳河逃生(即选择器官移植)。而河里至少有三条鳄鱼——排斥反应、感染、生物适配。羚羊要靠前后腿共同发力过河:前腿是基因编辑,后腿是免疫抑制剂。
NBD:“前腿”基因编辑有哪些限制?
陈忠华:目前基因修饰的数量从一个到几十个不等,像eGenesis,对猪进行了多达69个基因的修饰。
美国eGenesis公司宣传语:不让任何一个人在等待名单上死去
图片来源:官网截图
但是,基因编辑并不一定越多越好。我们的合作团队在动物实验中发现,敲除一个基因后,机体可能会通过修复机制产生新的抗原,并有可能刺激新的抗体产生。再者,过度改变基因会破坏物种的基因生态平衡,导致猪出现畸形、发育不正常、流产等问题,且技术难度极大。
另外,即使是经过相同基因编辑的猪器官,在不同的实验中表现也不一致:有的快速排斥,有的长期存活。这与个体差异、免疫抑制剂耐受度等多种因素相关,说明基因改变并非百分之百可靠有效。
单基因好还是多基因好?这个问题很难回答。如果一开始就将多个基因组合应用,就无法确定是哪一个基因起到了关键性作用。要搞清这点,需要把多个基因拆分开,用排列组合的方式,一一做独立的动物实验和人体实验,这几乎不可能完成。
所以,目前的多基因编辑就像我们吃中药一样,里面有很多种成分,如果能够治好病,具体也不知道是哪个成分起到关键性作用。
目前,不同公司、不同研究中心使用的猪器官基因编辑数量略有不同,样本量都十分有限,就像“盲人摸象”,无法得出哪种基因编辑组合更好的结论,需要更多样本和更长时间的研究才能做出判断和进一步优化。
NBD:“后腿”免疫抑制剂的问题有哪些?
陈忠华:目前美国食品药品监督管理局(FDA)批准了3个注册性临床试验,患者治疗过程都不太顺利,病情反复。这是因为,免疫抑制剂用量过多会引发感染,还可能对肝肾功能造成毒性损伤。部分患者移植器官功能不佳,并非完全因为排斥反应,而有可能是药物中毒和/或用量不足,无法有效控制排斥反应。
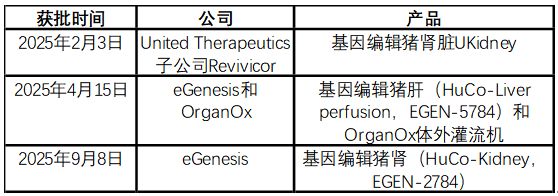
目前美国FDA批准了3个注册性临床试验图片来源:每经记者据公开资料制图
一方面,目前使用的免疫抑制剂都是为同种器官移植研发的,没有针对猪与人的物种差异设计,作用靶点不够精准、效果有限。缺乏专门针对异种移植免疫反应作用靶点的新药,这是当前具有挑战性的问题。
另一方面,目前异种器官移植的样本量太少,每个样本都需要用最新科学方法仔细分析,才能为研发新药物、新靶点提供依据。
NBD:为何中国还没有类似的注册性临床试验获批?
陈忠华:中美在异种器官移植管理上存在三个主要差别。
一是审批机制。中国目前没有专门的受理机构、统一标准和审批渠道,研究者发起的临床试验(IIT)研究多由医院自行发起,经内部同意后各自开展。
二是发展状态。国外通过严格标准规范研究,历经30年准备才重启新一轮临床研究;中国缺乏统一管理,发展相对无序。部分有基础的医院因为没有审批渠道,或者态度谨慎而迟迟未能推进,部分医院则积极开展相关研究。
三是政策支持。FDA鼓励申请,主动提供标准指导;国内各主管部门虽有主导意向,但尚未形成具体的审批流程和方案,处于相对茫然的状态。
人工器官路径分化:心脏接近普及,肝肾替代仍道阻且长陈忠华曾说:“产业化医用器官,包括异种器官和人工器官,必将成为除人体捐献器官以外的源源不断的补充性来源。”
而从公司和产品获批数量来看,人工心脏(左心室辅助装置)似乎显示出赶超之势。历史上,全球共有3款人工心脏获得大规模应用,目前HeartMate 3在全球范围内占据垄断地位。目前,中国也有5家公司生产的6种人工心脏正在奋起直追。
对于人工肾脏,解放军总医院非植入性“可穿戴式人工肾”已经完成动物实验和初步临床试验,预计2027年进入市场;美国加州大学旧金山分校(UCSF)的研究团队研发的可植入式人工肾脏,则计划在2030年前争取PMA(FDA针对高风险Ⅲ类医疗器械设立的上市前批准程序)申报。
那么,在异种器官移植取得突破性进展前,是否可能被人工器官抢先一步?
NBD:您如何看待异种器官移植和人工器官的关系?
陈忠华:最近我有一个讲题叫“三驾齐驱”,即比较了同种移植、异种移植和人工器官在解决人类器官衰竭问题上的优劣势。
NBD:人工器官最新的发展状况如何?
陈忠华:单看人工器官,人工心脏的发展速度最快,中国目前有5家企业、6款国产左心室辅助装置获批上市,其中雅培的HeartMate 3在去年也获批进入中国市场。
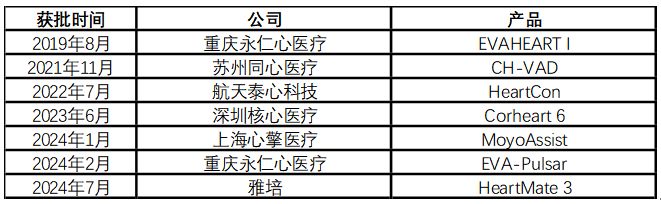
国内目前已有多个左心室辅助装置获批上市图片来源:每经记者据公开资料制图
据我掌握的数据,2024年人工心脏植入量达786例,直逼同年同种心脏移植量(1000余例);到今年5月,二者已基本持平。未来,大部分心衰患者可能会选择人工心脏,仅少数需要全心脏替代的患者仍依赖心脏移植——因为目前还没有开发出全心支持型的人工心脏。
然而,人工肾的发展则面临巨大瓶颈。自1943年第一台人工肾问世以来,小型化问题始终没有突破,无法实现体内植入,离临床应用还非常遥远。肝脏的生理功能复杂性更高,猪肝能产生大量核心功能性蛋白,因其结构上存在的异构特点,在人体无法发挥正常功能。目前普遍认为,猪肝(至少在现阶段)不是一个可植入的器官。可植入型人工肝脏的研究目前也还是空白。
总的来说,除心脏外,肾脏和肝脏的可植入人工器官目前还不具备与异种移植竞争的能力。
NBD:为什么人工肝脏和人工肾脏的开发更难?
陈忠华:因为磁悬浮人工心脏的小型化、AI控制等技术,完全可以解决血液分流等血液动力学问题,机械故障风险也能控制;但肾脏和肝脏在这方面的问题要复杂得多。
NBD:话说回来,您对于异种器官移植有什么寄语?
陈忠华:如今的异种器官移植,就像半个世纪前同种移植起步时一样困难,但存活时间正在逐步延长。我认为,只要突破一年的有功能存活关口,我们就有机会触及异种器官移植的本质,才有可能发现问题、寻找解决问题的方案并一步一步加以克服。直到出现稳定的长期存活案例,异种器官移植才会被急需救援的患者所接受。
在这个过程中,希望大家能体会到科学家的严谨,做一件事情就得有一定的基础,前人的经验,无论来自成功还是失败,都是值得借鉴的。

