西安大恒制药有限责任公司(简称西安大恒制药)涉生产、销售劣药一案,原本已于2025年4月由西安铁路运输法院执行局依法强制执行。近日,西安大恒制药收到的西安铁路运输法院执行裁定书显示,因涉案标的额大、案情重大复杂,依照《行政诉讼法》《民事诉讼法》之相关规定,裁定中止该案的执行。
这桩涉案金额巨大的劣药案,最早可以追溯至2019年5月。陕西省药监局接到举报称西安大恒制药“在药品生产过程中违反处方工艺,擅自添加辅料”。经立案调查,陕西省药监局认定该公司在2016年至2019年三年期间违规生产劣药,于2021年1月对其作出行政处罚,处没收劣药181800盒;没收违法所得、罚款合计4.4亿元。
针对上述行政处罚,西安大恒制药依法向陕西省政府提起行政复议,该处罚被维持。该公司遂向法院提起行政诉讼,2023年年底,该案经二审裁定维持原定行政处罚。
因该案判罚金额巨大,且一审及二审结果呈现反转,故备受关注。涉事药企并已向相关法院申请再审。
273份证据存在数量缺失等问题
西安大恒制药位于西安市高新区,成立于2002年,原为国企控股,2013年改制为民企。该公司曾拥有180名职工,年产值1亿元,主产阿奇霉素软胶囊、克拉霉素软胶囊等软胶囊药品及其它片剂、硬胶囊剂等。
根据陕西省药监局对西安大恒制药的行政处罚,省药监局认定,自2017年1月至2019年3月期间,西安大恒制药生产的273批次阿奇霉素软胶囊和克拉霉素软胶囊在生产时违规添加辅料。
西安大恒制药相关负责人向界面新闻记者表示称,涉案辅料PEG200与吐温80均为《中华人民共和国药典》法定药用辅料。2019年4月-5月,公司GMP证书到期,处于停产整改期,遂安排两款药品进行工艺辅料变更稳定性实验,(目的是把阿奇霉素软胶囊和克拉霉素软胶囊目前的有效期18个月延长为24个月)。具体做法是在阿奇霉素软胶囊实验中,将原批生产处方中辅料聚乙二醇400(PEG400)从109kg减少为95kg,另外增加了PEG200 14kg。从化学本质看,PEG400与PEG200同属环氧乙烷聚合物,基础分子结构单元一致,加入PEG200后不会产生新的物质,且更易溶解,流动性更好。在克拉霉素软胶囊生产实验中,添加吐温80的作用是可以有效提升产品有效期且不改变原有的质量标准。
上述负责人向界面新闻强调,上述添加涉案辅料的实验所用药品(三批阿奇霉素软胶囊、三批克林霉素软胶囊)均未制成成品,亦未投入市场,“(这些)没有一颗药流入市场”。公司向法院提交的全国各级药品监督管理部门出具的多份《合格报告》,均能说明上述事实。
庭审资料显示,2019年5月28日,省药监局在西安大恒制药现场提取实验记录本和实验领补料单;2019年6月10日,省药监局再次在公司现场提取84批阿奇霉素软胶囊、189批克拉霉素软胶囊的正式生产记录和领补料单。
两种涉案药品的实验数据也被省药监局在一审中作为关键证据进行了提交。判决书显示,省药监局的证据主要包括:两种药品的新药证书、注册及再注册批件、药品标准、药品研究实验记录、领补料单、询问笔录等。
“省药监局共计向法庭提交了273份药企的生产记录作为证据。其中,有181份是在真实的批生产指令单后面,拼接了实验记录中的领补料单,但是实验用领补料单无进厂编码,是我们仅做实验参考用的;其次,药监局共处罚了84批次阿奇霉素软胶囊、189批次克拉霉素软胶囊,但提交的证据缺少6批次的阿奇霉素和6批次的克拉霉素的生产记录,也就是说核心证据就少了12份;另有37批领补料单显示辅料领用量显示为零。”上述负责人表示。
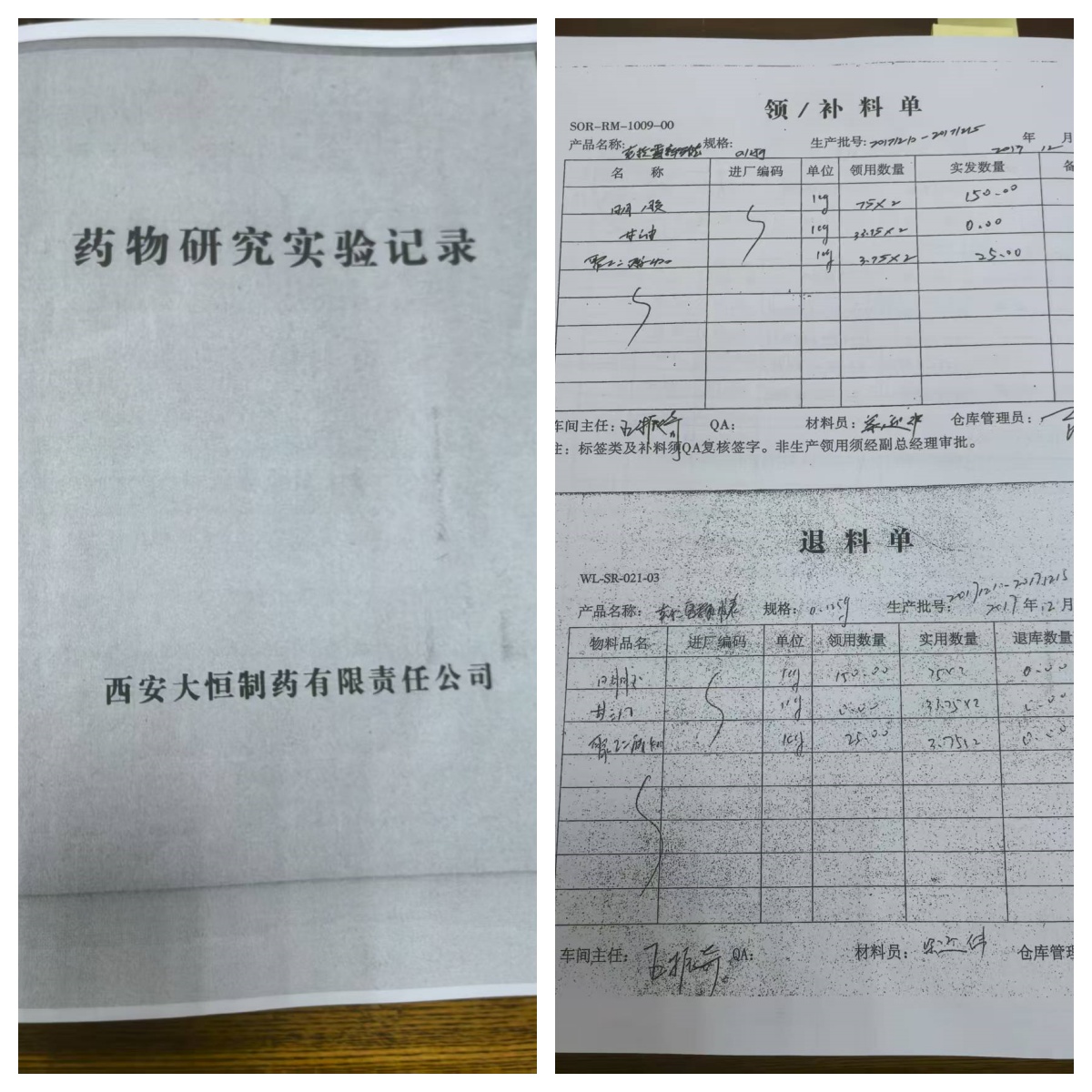
西安大恒制药实验记录和领补料单。图片来源:一审庭审资料
西安大恒制药也在一审过程中提出,对上述证据的真实性不认可。一审庭审资料显示,西安大恒制药称,省药监局提供的领补料单、退料单无进厂编码,与原告一式三联的生产记录完全不符。其自行制作的货值金额统计表作为认定原告的违法所得及罚没金额的依据的最重要的证据均为被告自行制作,没有原告确认,被告在作出行政处罚中多处证据存在认为拼接的情况。
经一审法院认定,案涉行政处罚决定书认定事实不清、主要证据不足、程序严重违法、适用法律错误,依法应予撤销并重新作出处理。
法院认为,经庭审举证、质证的证据证实,陕西省食品药品监督检验研究院和西安市食品药品检验所的多份检验报告证实,案涉的阿奇霉素、克拉霉素软胶囊在2018年7月30日、2018年8月10日、2019年8月16日等3次检验结果均为“结果符合规定”。而陕西省药监局却将大恒制药在2017年1月1日至2019年3月30日间,生产的84批次阿奇霉素软胶囊和189批次克拉霉素软胶囊全部认定为劣药,其证据之间存在矛盾,故应由陕西省药监局重新调查、核实。
实验数据能否作为定罪证据?
一审判决出炉后,西安大恒制药与陕西省药监局双双选择了上诉。二审过程中,此案争论焦点主要在——关于劣药的认定问题,原《药品管理法》(2015版)与《药品管理法》(2019版)有所不同。
判决书显示,省药监局称,大恒制药的违法行为是在药品生产过程中违反处方工艺,擅自添加辅料,应适用《药品管理法》(2015)第四十九条第三款“有下列情形之一的药品,按劣药论处,”第五项“擅自添加着色剂、防腐剂、香料、矫味剂及辅料的”,根据该项规定,只要认定药品生产企业存在擅自添加辅料的行为,无论是否检验,无论检验结果如何,均应定性为劣药。因此,虽然上述3批次涉案产品检验均为“结果符合规定”,但并不影响其劣药的定性。其次,药品检验只能依据药品标准进行,而药品标准只规定了药品中所含主要成分的检验方法和要求,不可能对药品中任意违法添加的各种物质一一作出具体检验规定和要求,因此,违反生产工艺、添加辅料不必然导致“检验结果不符合规定”。
西安大恒制药则认为,按照新法之规定,擅自添加辅料的药品为劣药,但对劣药的处罚决定,应当依法载明药品检验机构的质量检验结论。
2024年11月15日,西安铁路运输中级法院的二审判决给出了最终定论:法院认定,引发争议的行政处罚决定书事实清楚、证据确凿,且在针对涉案法人的处罚程序上符合法律规定。因此,法院裁定维持原行政处罚决定。
二审法院认为,关于假药、劣药的认定问题,本案争议焦点在是否适用原《药品管理法》(2015版)、《药品管理法》(2019版),以及《最高人民法院最高检察院关于办理危害药品安全刑事案件适用法律若干问题的解释》。对此,法院认为,药品质量检验结论并非为认定违法行为的必要证据。对本案这种没有按照批准处方投入辅料生产药品的,即属于擅自添加辅料,对擅自添加辅料这一事实认定问题,是不需要通过药品检验结论这一证据来认定的。
界面新闻记者注意到,一、二审法院具备共识——关于假药、劣药的认定问题,并非必须载明药品检验机构的质量检验结论,而是主要依据药企在药品生产过程中是否存在违反工艺的违法行为。
那么,药企为提高药品保质期而进行的研究实验,省药监局能否将实验记录作为该案的核心证据?
山东一家上市药企董秘向界面新闻记者表示,“药品研究实验记录能否作为企业生产劣药的证据,关键要看涉案药品是否流入市场形成销售,也即是否对消费者造成有害影响。另外,一般情况下监管对于类似劣药案的认定,都需出具涉案药品的质量检验报告。公司曾经有一家合作药企,就是因为违规生产药物流入市场,并且有相关质量检验报告,而被监管部门认定生产、销售劣药罪。”
多名法律界人士向界面新闻记者表示,以实验数据替代正式生产数据对企业进行巨额判罚的劣药案,在全国范围内也并不多见。
界面新闻查询发现,存在类似劣药案判例,因涉案药品实验数据不足以认定药企生产“假药”,监督部门后续撤回了行政复议申请。
云南省司法厅官网2024年6月14日发布的《行政复议行政诉讼十大典型案例》显示,2022年8月,国家药监局通告某药企生产的一批中药材不符合《中国药典》的性状和鉴别标准。云南省药监局于2023年3月作出行政处罚,认定该批药材为“假药”,没收药品并罚款50万元。
在行政复议期间,复议机关(云南省司法厅)与省药监局反复沟通后,省药监局主动承认以下问题:一是实验数据与结论的关联性不足:检验报告仅显示药品成分与标准不符,但未证明该成分对人体有害或影响药效。二是法律适用错误:根据《药品管理法》,“假药”需具备“成分不符”或“冒充药品”等法定情形,但本案中实验数据无法直接支撑 “成分不符” 的认定(因未排除地域标准差异等因素)。云南省药监局于2023年6月自行撤销原处罚决定,并重新启动调查程序。药企随后撤回行政复议申请,案件终止。

