【这两天股价大跌的原因找到了:公司需要计提董秘沟通能力这笔商誉】 事实上,公司的董秘沟通能力与新药研发能力形成了巨大反差,前者已成为公司的一大笔负资产,不得不计提的一大笔商誉,后者则是公司崛起成为世界级创新药企业的基石。敬请投资者【高度关注上述风险,慎重决策】。
附:请问董秘,公司会准时提交补充材料吗?常山药业:尊敬的投资者,你好。公司已经提交了艾本那肽上市审评需要的补充资料,后续有形式审查、补充资料审评等环节,预计有较长时间才能进入网上公示补充资料审评进展阶段。艾本那肽上市审评后续环节仍然较多、审评时间仍然较长,最终审评结果及完成审评时间存在不确定性。请投资者高度关注上述风险,慎重决策。股票市场价格可能因多种因素而波动,这些波动并不完全反映本公司的经营状况。请投资者理性投资,注意投资风险。(来自深交所互动易 答复时间 2025-11-03 15:00:12)
特别要注意,投资者的提问是——“请问董秘,公司会准时提交补充材料吗?”
公司的回复本可以简明扼要,实际上却是不厌其烦说了一大堆的话——“尊敬的投资者,你好。公司已经提交了艾本那肽上市审评需要的补充资料,后续有形式审查、补充资料审评等环节,
预计有较长时间才能进入网上公示补充资料审评进展阶段。
艾本那肽上市审评后续环节仍然较多、审评时间仍然较长,最终审评结果及完成审评时间存在不确定性。请投资者高度关注上述风险,慎重决策。股票市场价格可能因多种因素而波动,这些波动并不完全反映本公司的经营状况。请投资者理性投资,注意投资风险。”
【请投资者高度关注上述风险,慎重决策。】——这句话意味深长。从董秘来说,按职业操守的要求,在这里的表述既可以采用【关注】两字,也可以采用【高度关注】四字,而实际上董秘选用【高度关注】,其良苦用心近乎“此地无银......”
(2025-11-03 20:21:40)
龙城旭日东升
2025-11-04 18:53:16来自 山西:
这个董秘一直有问题,就想左右股价为主力服务!另外前后矛盾,前面说交资料去药监局查,现在怎么自己说又添油加醋!
熠熠生钱2025年11月04日 19:39 浙江:
昨天看到董秘的回复互动,心理就咯噔一下,想着明天做好5个点的回撤,谁想又是20cm。但凡是10个点我也不说了,又是跌停这就有点不讲究了。
董秘(或者公司),我觉得你是通过投资者互动平台来喊话操控股价,你其实直接回复补充资料已经上交就行了,如果要多说点,那就说审批时间有不确定,审批结果也有不确定性。而你的回复带有明显的引导倾向。1、预计有较长时间才能进入网上公示补充资料审评进展阶段,审评时间仍然较长。何为较长时间?一个月算长还是算短?如果是好几个月,那你们这么早打预付款买艾本那肽的原材料就是为了让三季报不好看吗?你们这么早就开始招聘销售人员是因为销售专业性很强需要大半年的培训时间吗?2、请投资者高度关注上述风险,慎重决策。你一边让我们高度关注风险,一边又说对自己产品有信心而且还有几次论坛上专业人士的解读。你是先骗投资者进来,然后最后为甩锅埋下伏笔吗? 如果不是,你表达了不确定性就行了,需要用高度关注这个用词吗?
宁波第一深情 2025年11月04日 19:18 浙江:
其实董秘每次回复不是随便找个时间回复的,这里面大有学问,自己品。
txdyn 2025年11月04日 13:46 湖北:
涉及多少项目,也就是有几盏灯会亮,然后等灭灯。这也是昨天董秘所说,预计有较长时间才能进入网上公示补充资料评审进展阶段。
——这样的解读,就是董秘文字表述不严谨引起的。【预计有较长时间才能进入网上公示......】有别于(需较长时间才能完成补充资料审评进展阶段)。
常有金山2032025-11-05 11:44:55来自浙江:
按董秘回复的字面理解,网上公示审评进展似乎是在补充资料审评结束后,这才合乎董秘说的需要较长时间的逻辑。形式审查按规则只需5个工作日,不可能是较长时间。如是等待公示出来就已是资料审评完成进入行政审批阶段了。这样看来这个补充资料的审评是非常规的,很特殊。
点评:按董秘回复的字面理解?董秘回复的那句话【预计有较长时间才能进入网上公示补充资料审评进展阶段】,本身就是无法准确理解的,因为这句话有语病。据说董秘有大专文凭,但可以绝对肯定非中文系专业毕业,不然就对不起那张文凭。
守住常山就是金山银山 2025年11月05日 14:56 湖北:
常山药业公司今年两次(06.09、11.03)在公司股价上涨途中提示风险,均造成股价的大幅下跌。公司是否有故意操纵股票涨跌为利益方谋利的行为?因为在两次的公告中,它存在一些暗示性极强、故意诱导市场的提法:“如后续股票交易进一步出现重大异常,为保护中小投资者合法权益,公司将依规申请停牌核查。”“请投资者高度关注上述风险,慎重决策。股票市场价格可能因多种因素而波动,这些波动并不完全反映本公司的经营状况。请投资者理性投资,注意投资风险。”而且两次公告均造成股价的实际大幅下跌,明显有配合资金打压股价的嫌疑。
g292652i962025-11-05 11:10:01 来自 辽宁:
公司应该气象一新,管理层也要做相应调整,包括董秘。因为常山要与国际上大公司PK的话,公司人员的素质学历经验就必须要更高一些。
点评:这个建议可以有。
c13333714196457172025-11-05 21:21:09来自云南:
什么叫带节奏,这二十个点,还看不懂?你们做什么票,做多久了?公告不发,一个董秘回复跌这么多,是批不过还是药试验数据有偏差。如果这都可以跌20个点,那这个票真的是,趁早出局,不要做了,没有一点欲望想做这个票。
金马时代2025年11月05日 20:41 湖北:
从暴涨到跌停:常山药业用惨痛教训告诉我们,好公司更需要好沟通。
(续前)“再涨就停牌! ”这几个字从常山药业的公告里蹦出来时,很多投资者都愣住了。今年6月中旬,因为股价连续两天涨幅超过30%,公司居然用停牌来威胁市场。 结果没几天,6月19日开盘不到半分钟,股票真的被打到跌停。时间跳到11月3日,苦等已久的“发补”资料终于在截止前第76个工作日提交了。按理说这是好事,可董秘的反应让人心凉半截。他没有和股民一起高兴,反而泼冷水说......得,第二天股价直接低开,最后20%跌停收场。对比一下通化金马,人家也在新药审批的关键阶段。 他们的董秘是怎么说的? 说新药“已经完成各项专业审评工作进入综合审评环节”,“处于临近审批阶段”。 这话听着就让人踏实。 结果常山药业暴跌那天,通化金马只微跌了零点几个点。
(续前)有投资者在网上发问:涨30%就威胁停牌,那要是连续两天跌30%,公司是不是也该有个说法? 这个问题,现在还没有答案。
股市本来就是个放大情绪的地方。该安静的时候指手画脚,该说话的时候装深沉,这样的公司确实让人寒心。散户们抱着价值投资的理念来,想着做“耐心资本”,结果遇到这种驱赶式的暴跌,换谁都难受。
通化金马的例子说明,同样的事情可以有更好的处理方式。 投资者关系管理不是可有可无的装饰品,而是上市公司必修的内功。药好固然重要,但让投资者安心同样关键。
不妨翻翻本人以往的帖子——2025年09月16日 16:41 【细心人应该可以发现:公司方面多次提示投资者不要过度解读一些事情】 。但这次不能不把董秘推上前台说事,因为董秘过度反应或刻意带节奏了,这显然是突破了职业操守。
基民wTszyV2025-11-06 08:58:14来自江苏
本来是从从容容游刃有余,现在是匆匆忙忙连滚带爬,董秘睁眼说瞎话,没出息。
股友31V6Q086162025-11-06 08:25:07来自河北:
这个董秘就是一把悬在小散头上的达摩利斯剑!!!!!
浙江有为青年 2025年11月07日 08:35 浙江:
关于药审中心公示表格中数据解读——
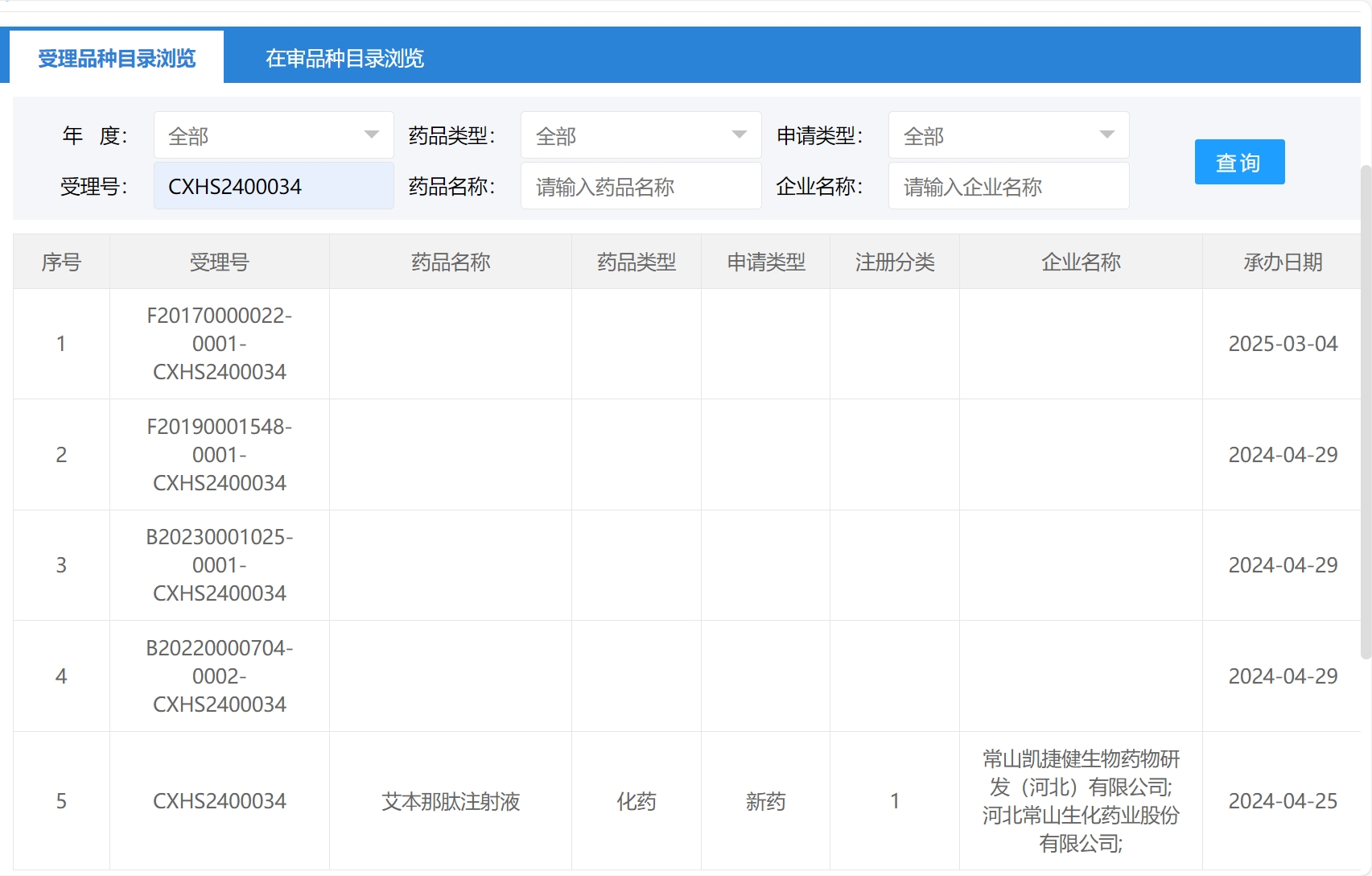
前四条记录是第五条记录(CXHS2400034)相关联的审评流程。它们共同构成了“艾本那肽注射液”这个新药上市申请(NDA)的完整审评卷宗。前四条记录,它们的共同点是都后缀了主受理号“-CXHS2400034”,这明确指出了它们与主申请(艾本那肽注射液)的从属关系。在中国国家药监局(NMPA)药品审评中心(CDE)的系统中,这种编码方式通常用于 “关联审评”。根据中国现行的药品注册法规,一个成品药(如艾本那肽注射液)的上市申请,需要将其相关的原料药、辅料、直接接触药品的包装材料等信息一并提交并进行审评。这些关联的物料申请会获得一个与主申请关联的受理号。记录1和2(F字头):是“艾本那肽注射液”所使用的两种关键辅料。它们可能早在2017年和2019年就已经在CDE平台完成了登记,现在被关联到本次新药申请中。记录3和4(B字头):是“艾本那肽注射液”的原料药 部分。B20230001025可能是艾本那肽原料药本身,而B20220000704-0002可能是一个相关的中间体、或者另一种规格的原料药。
关联审评的启动,明确表示“艾本那肽注射液”已经完成了临床研究,正式进入了上市许可申请的审评阶段。这是药物研发管线中价值兑现的关键一步。关联的原料和辅料信息表明,公司已经确定了产品的最终生产配方和供应链。这对于评估未来产品的生产成本、质量稳定性和规模化生产能力至关重要。通过关联审评,将原料药、辅料和制剂一次性审评,可以系统性评估产品的质量,降低了未来因供应链上某一环节问题而导致上市后变更或召回的风险。
火星熔橙2025-11-06 23:52:18 来自 广东:
第5序列号是第一炮适应症二型糖尿病患者,第2一4序列号是第2一4炮适应症阻塞性睡眠呼吸暂停(OSA),慢性肾脏病(CKD),代谢功能障碍相关性脂肪肝病(MASH),神经退行性疾病等。这次审批有可能通过的就以上序列号2.3.4.5,而第1序列号减重适应症还没有临床应该是通不过了。
到手的才是利润2025-11-07 08:45:18 来自 安徽:
减肥临床是4月10申请,6月份获批,你这承办日期对不上,补充资料的可能性更大一点。
占卜师在常山采风2025-11-07 08:02:55 来自 重庆:
补充的部分,已在审!
仰望海上的星空 2025年11月05日 09:10 四川:
管理层一通操作下来,直接把市场信心给按住了。其实,股票这东西最怕的就是市场没信心。当你的董秘一通负面指引,大家还敢买吗?难怪,常山药业成了“创新药股票中唯一两次20%跌停”的奇葩代表。
zjf梦润2025-11-04 20:17:48 来自 江苏:
估计董秘和资本勾结,昨天高位卖了,然后董秘无话找话通过e互动打压股价。常山药业董秘通过回答股民而左右股价。回答问题前后矛盾。
我姓唐2025-11-07 12:07:49来自浙江:
审评进行中。不处理发不出来。
价值投资与投机作者
2025-11-07 12:42:36来自 浙江:
证明开始审批了。
有教养的心
2025-11-07 12:30:56来自 上海:
辅料、包装之类的,跟补充材料有关,一起重新审了,等于艾本的材料已经在药监速度开审了, 一步步来。快了,前面几次暂停补充,这把应该没问题了。主力暴力砸跌停,也是因为时间不多了,抓紧震。
JUVENTUS12025-11-07 10:49:31来自江苏:

txdyn 2025年11月07日 18:32 湖北:
四个新出现的关联受理号进入“在审目录”意味着什么?结论:这意味着针对艾本那肽注射液发补资料的、全面的、多模块的技术审评已经正式启动。
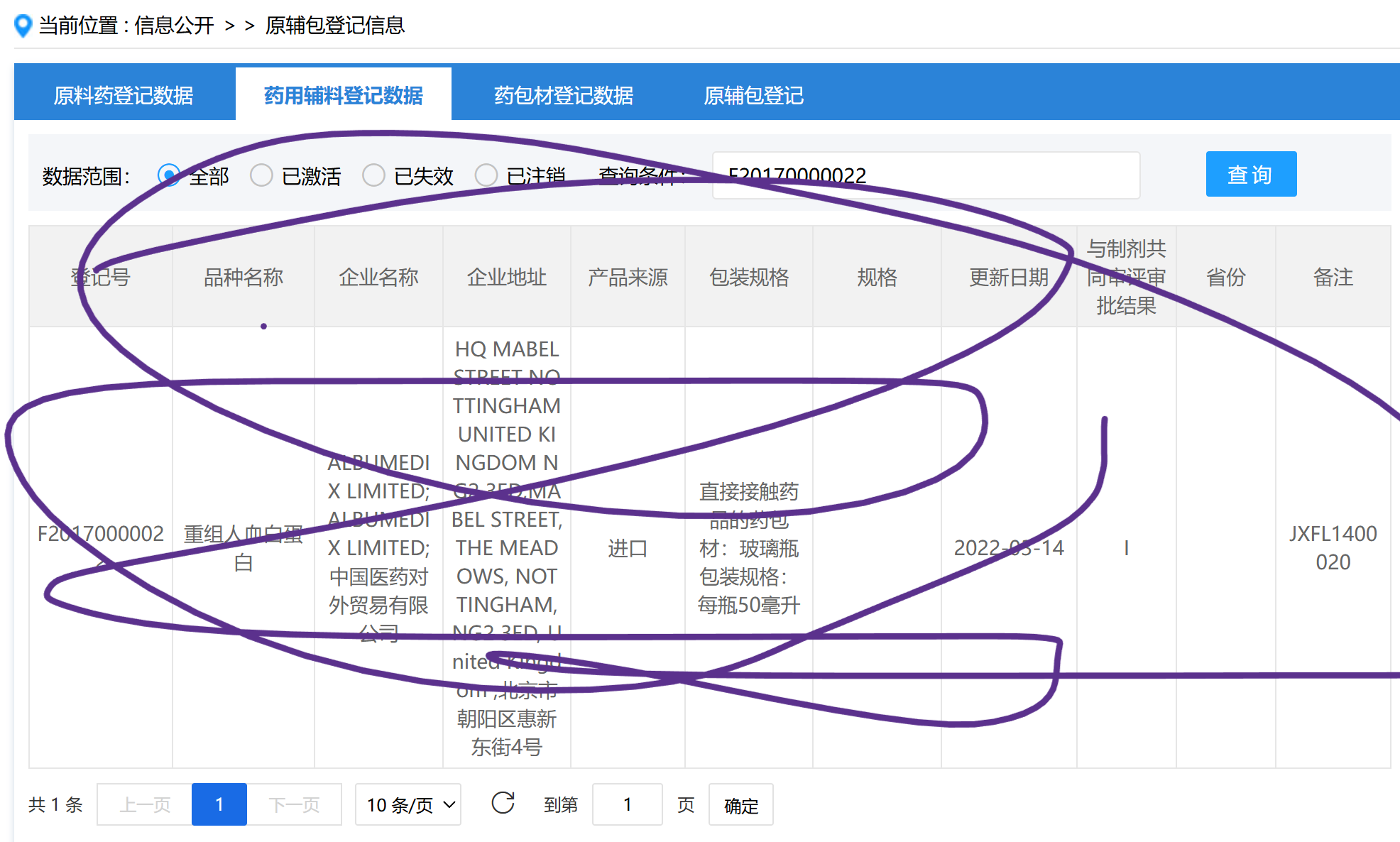
(续前)这4个受理号(F20170000022, F20190001548, B20230001025, B20220000704)分别对应的是艾本那肽注射液的 “原辅包”(原料药、辅料、包材)和 “给药装置”。
F20170000022 - 重组人血白蛋白:这很可能是艾本那肽的原料药。一个创新药的原料药需要单独登记和审评,确保其来源、质量、纯度符合标准。
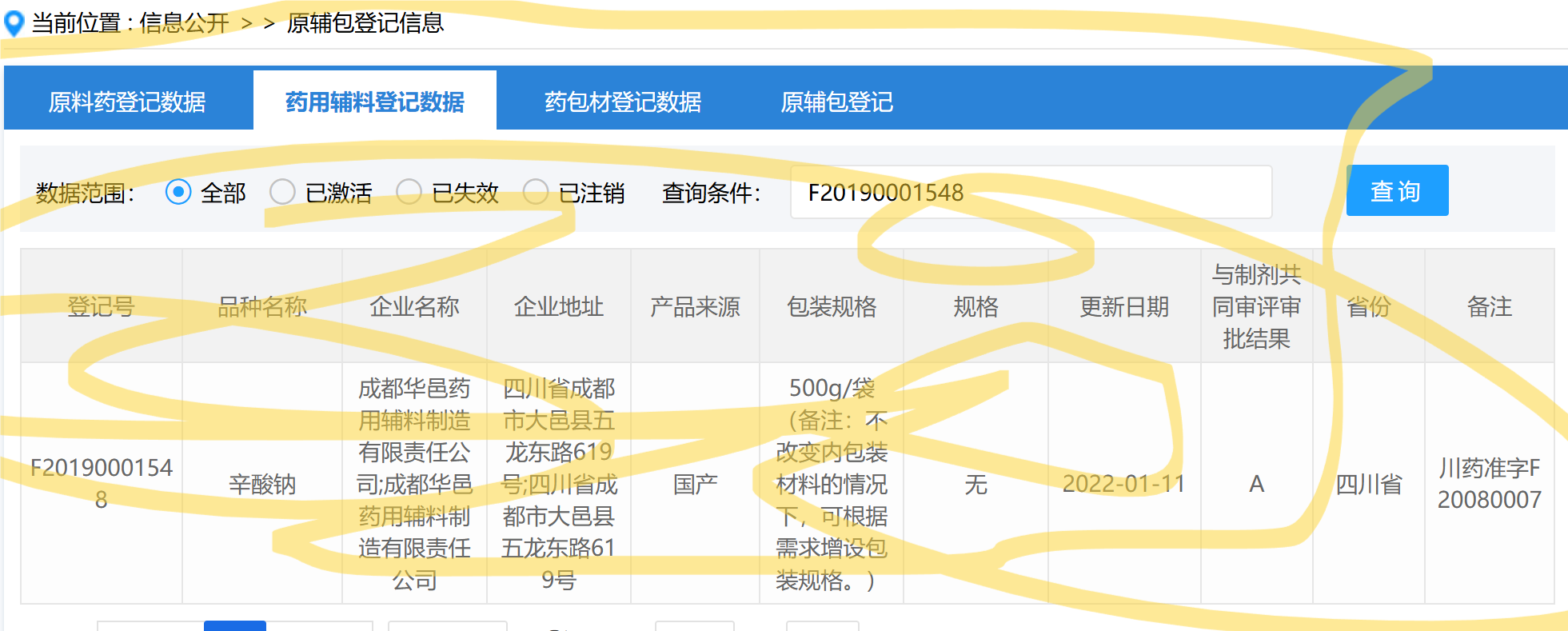
(续前)F20190001548 - 辛酸钠:这是一种药用辅料,在制剂中起到稳定药物、调节pH值等作用。它的质量和兼容性需要被审评。
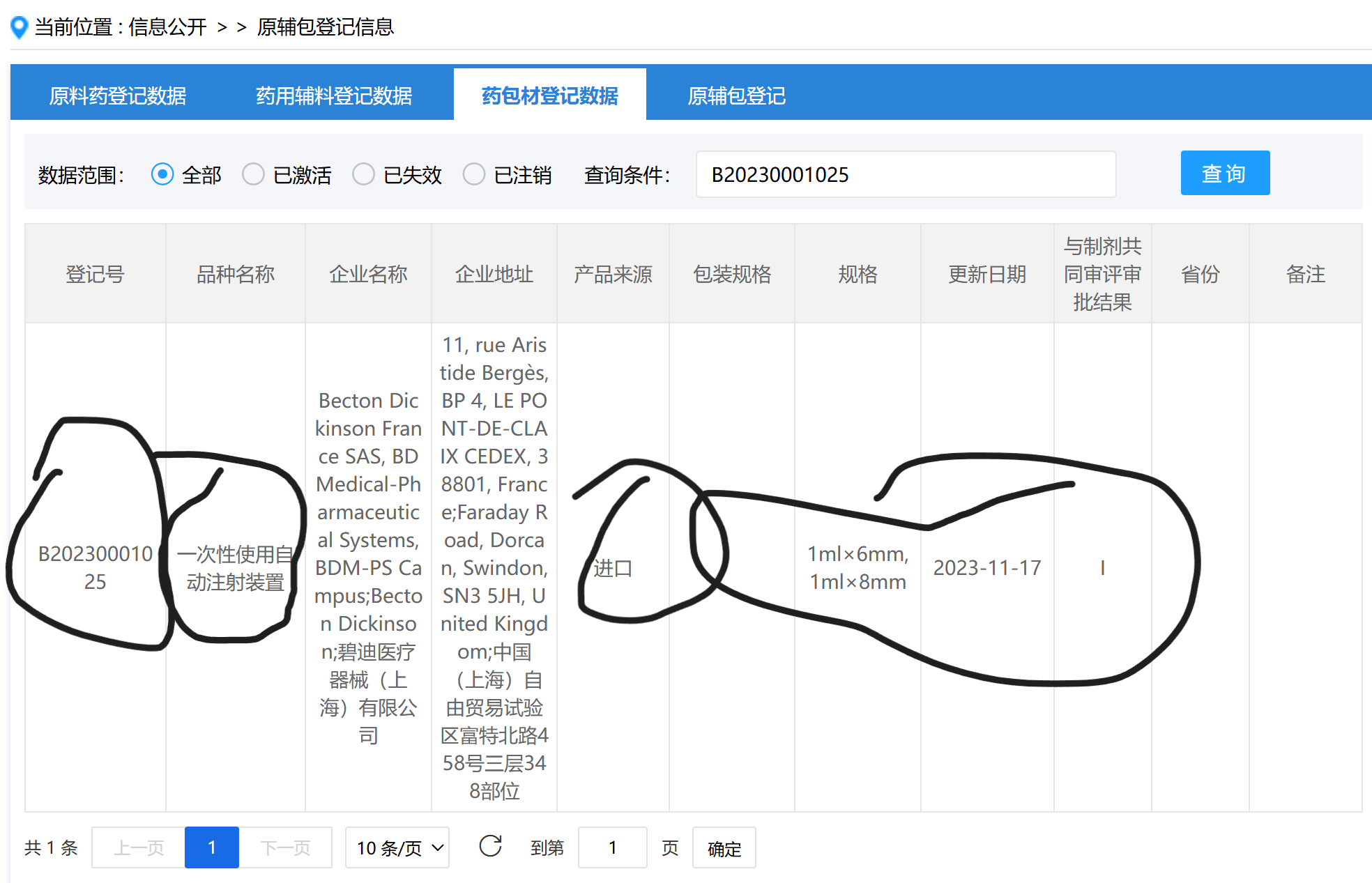
B20230001025 - 一次性使用自动注射装置:这是艾本那肽的关键给药设备(类似胰岛素笔)。对于这类生物制剂,便捷的自动注射装置是产品的重要组成部分,其安全性、有效性和可靠性需要与药品本身一同审评。
B20220000704 - 笔试注射器:这是另一种给药装置的选项或组件。公司可能申报了不止一种装置类型。
(续前)为什么它们同时进入“在审目录”至关重要?
因为这表明CDE的审评团队正在从“药品本体”(原料药、制剂配方) 到 “配套系统”(辅料、包装、注射装置) 进行全链条、同步的审评。这是一种 “制剂-原辅包”关联审评的模式,确保最终上市的是一个完整、安全、有效的产品。这是发补资料进入实质技术审评阶段的最明确信号。
(续前)为何“审评任务公示”里的“补充资料任务公示”还查不到?
这也是很多人会困惑的地方。这主要是由CDE内部工作流程和信息公开的时序性造成的。“在审品种目录”是状态标识:它更像一个实时或准实时的状态看板。一旦CDE确认收到企业的发补资料并分配给审评员,这个目录就会更新状态,显示为“在审”。这个动作很快。“审评任务公示”是计划公告:它需要走一个内部的确认和发布流程,可能会有几天的延迟。通常,CDE会定期(如按周或按批次)更新任务公示列表。简单来说:状态看板(在审目录)先更新,任务公告(补充资料任务公示)后发布。 您现在看不到是正常的,预计在未来几天到一周内,应该就能在“补充资料任务公示”栏中查看到艾本那肽的任务信息了。
(续前)艾本那肽(阿贝那肽)最终上市的可能性有多大?
基于目前所有公开信息分析,艾本那肽最终获得批准上市的可能性极高(超过95%)。理由如下:
1. 已进入“最后冲刺”阶段:发补是创新药上市申请(NDA)流程的最后一环。企业能提交发补资料,意味着前期核心的药学、临床前和临床试验数据已经通过了CDE的初步审查,没有发现颠覆性的问题。现在只是在就一些细节进行完善和确认。
2. 临床价值的认可:艾本那肽作为GLP-1类药物,用于治疗2型糖尿病,其临床试验数据已经证明了有效性和安全性。这是它能够走到发补阶段的基础。
3. 完整的产业链配套已就位:从查到的信息看,原料药、关键辅料、两种注射装置都已经登记在案并与制剂关联审评。这表明常山药业已经为规模化生产和上市销售做好了全部供应链准备。一家公司不会在供应链上投入如此大的资源,除非对产品获批有极强的信心。
4. 更名事宜的推进:“艾本那肽”更名为“阿贝那肽”是按照国家药典委员会的要求进行的标准化工作。这个工作的推进本身也说明药品正在向最终的上市标准靠拢。
(续前)综合研判与下一步展望——
目前观察到的现象,正是这款国产创新药在上市前 “临门一脚” 的关键时刻。当前阶段:全面技术审评期。CDE的多个部门正在同步审核发补资料。
下一关键节点:在 “审评任务公示” 中看到艾本那肽的补充资料任务信息。在 “优先审评公示” 中看到它的信息(鉴于其创新性,有可能被纳入优先审评,进一步加快流程)。
(续前)最终流程:技术审评全部通过 → 进入“行政审批”阶段 → 国家药监局(NMPA)签发药品注册批件。
总结:一切迹象都表明,艾本那肽(阿贝那肽)的上市申请正在按部就班、顺利快速地推进,目前已经进入了最后的审评环节,成功获批几乎是确定性事件。请继续保持关注,接下来的几周内应该会有更明确的任务公示信息。
我姓唐2025-11-07 13:46:12来自浙江:
这四个东西是艾本那肽的药用辅料和药用包材,根据药监局2019年的一个规定,在中国境内研制、生产、进口和使用的原料药、药用辅料、药包材的供应商都要在这里登记,并和申请上市的药品相关联。有关部门要对原辅包的技术资料保密 。一旦新药批准,意味着原辅包也通过了。原料药、药用辅料、药用包材在这里也仅仅是登记 ,登记人对登记信息的完整性和真实性负责。 只是不清楚,为什么最近艾本那肽的信息才和药辅包信息关联在一起。
轻松的许菡2025-11-07 18:08:50来自广东:
才发现常山的地址是正定县梦龙街71号,所以才收个71.71吗?主力是不是有点强迫症?还是说纯巧合呀?
txdyn2025-11-07 19:27:50
有人质疑承办时间是过去的问题,在正常情况下,这些申请可能已经存在,但在企业提交发补资料前,它们可能处于“暂停”或“待审”状态,在公开列表中不显示或排在后面。此次变化的直接触发点,就是常山药业在11-03提交了发补资料。 这一动作意味着:
资料齐备,时钟重启:CDE确认企业提交的发补资料齐全后,正式重新启动了针对这4个技术模块的审评流程。
状态更新:因此,这4个受理号被重新激活并推到了“在审品种目录”的前列,状态更新为“正在审评中”,所以它们“新出现”在列表顶部。
追日逐梦 2025年11月08日 10:53 湖南:
常山药业艾本那肽升级版阿贝那肽审评上周已开启,细心的人会发现补充资料内容却是辅料(比如重组人血白蛋白、注射器等一些基础资料审评),与常见发补审评大相径庭。
重复之前的预判:阿贝那肽通用名称的变更以及相关的补充资料的补充申请(技术性发补),和常见的发补(专业性发补)完全不同。阿贝那肽的技术性发补虽很繁琐,但不会失败,因为技术性发补不涉及已完成综合审评的专业审评,仅是需要完成与阿贝那肽更名相关的程序资料补充而已。虽然在药监局官网中都是“补充申请审评”,却有明显不同,上周一堆F开头CXHS2400034结尾的补充申请资料更新公示表明,99.99%的人理解错了,此“发补审评”不是彼“发补审评”,补充申请审评早已开始,当药监局官网出现一堆阿贝那肽之时,就是批准上市之时,没有了灭灯可查,也不会有行政审批了。因为F开头和B开头的补充申请就是行政审批内容。
点评(特别提示):迄今为止公司公开披露的信息(互动回复)都不同于上述说法。
我姓唐 2025年11月08日 22:50 浙江:
根据药监局《关于进一步完善药品关联审评审批和监管工作有关事宜的公告(2019第56号)》的规定,申请上市的药品的原料、辅料和包材信息都要在登记平台进行登记 。艾本那肽相关联的二个辅料二个包材信息就是按照这个要求进行的登记,但之前没有放在一起。2017年就有同样的规定,但只针对仿制药,2019年药监局上述公告要求创新药也要登记原辅包信息。药监局审评中心有一个“原辅包登记信息”的栏目,里面有几万条申请上市药品的原辅包登记信息。我的问题是,以前艾本那肽和辅料包材信息为什么没有放在一起,出现什么情况才放在一起。药监局一年大概批准40多款1类创新药(其中23款化药,其他是治疗用生物制品和中药),能查到放在一起的不多,比如,CXHS2300107、CXHS2400046、CXHS2400073、CXHS240084,等。很多获批了都没有放在一起。
然毅自由2025-11-09 02:50:29 来自 广西:
(回应楼上)通化金马的也有了。

