艾本那肽注射液最新情况排列第6位
艾本那肽注射液最新情况

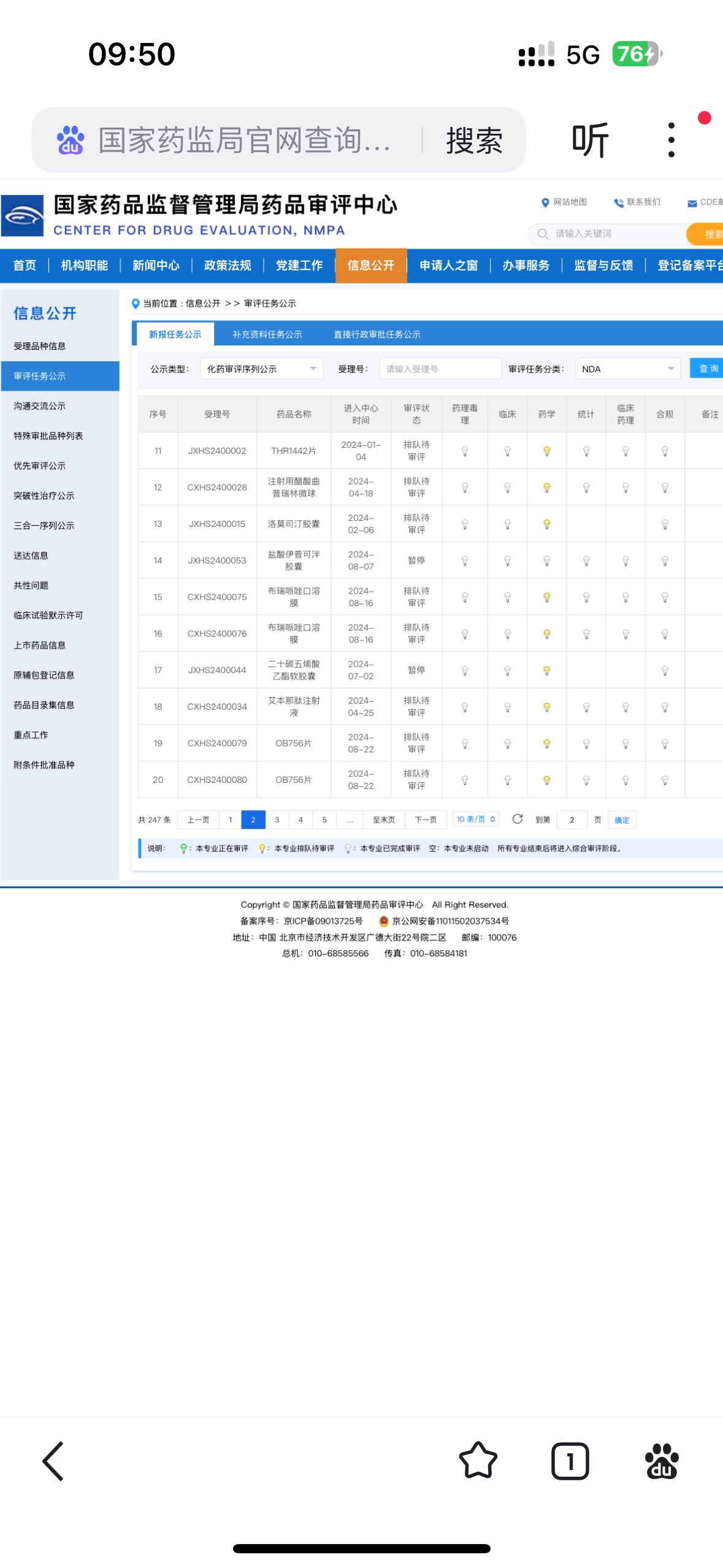
排列第6位
2025-05-20 10:06:16 作者更新以下内容
IND和NDA的定义和区别
- IND:新药临床试验申请,主要用于在人体上进行试验前的准备工作。IND申请的目的是确保药品在人体试验中的安全性,并验证临床方案设计的合理性。IND申请需要提交包括药理研究、动物急毒试验等在内的研究资料,一旦FDA在收到IND申请后30天内未提出反对意见,申请人即可自行开展新药临床研究。
- NDA:新药上市申请,用于新药完成所有临床试验后,申请上市注册。NDA的主要目的是确保上市药品的安全、有效和质量可控。NDA申请需要提交详细的临床研究数据、药代动力学数据等,以证明药物在人体内的安全性和有效性
郑重声明:用户在财富号/股吧/博客等社区发表的所有信息(包括但不限于文字、视频、音频、数据及图表)仅代表个人观点,与本网站立场无关,不对您构成任何投资建议,据此操作风险自担。请勿相信代客理财、免费荐股和炒股培训等宣传内容,远离非法证券活动。请勿添加发言用户的手机号码、公众号、微博、微信及QQ等信息,谨防上当受骗!
评论该主题
帖子不见了!怎么办?作者:您目前是匿名发表 登录 | 5秒注册 作者:,欢迎留言 退出发表新主题
郑重声明:用户在社区发表的所有资料、言论等仅代表个人观点,与本网站立场无关,不对您构成任何投资建议。用户应基于自己的独立判断,自行决定证券投资并承担相应风险。《东方财富社区管理规定》

