(血液制品上市公司主要产品批签发数统计 一)
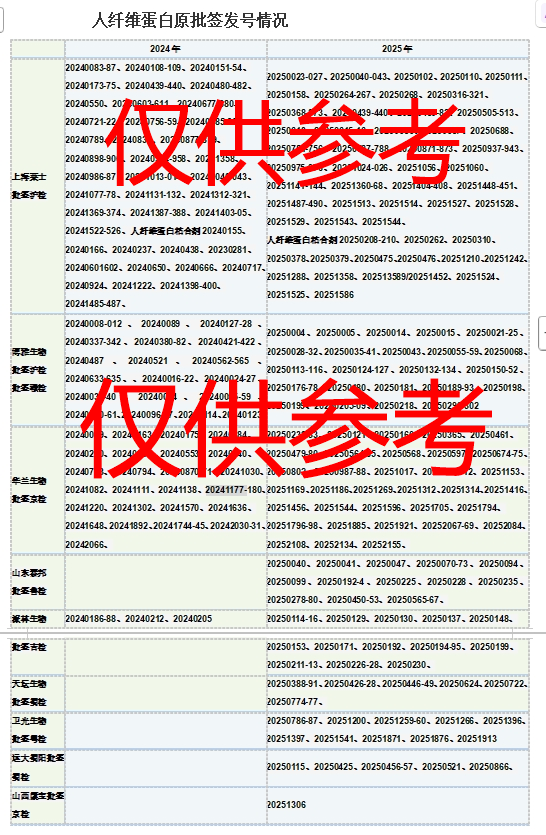
根据博雅生物财报数据,人纤维蛋白原毛利率稳居60%以上,各大血制品生产企业均加快了研发生产步伐,已取得生产许可证的企业都在挖掘潜力,提高产量。从前几年检验机构公布的《生物制品批签发产品公示情况汇总》来看,广东所要3月初,上海所要2月下旬才能公布完前一年批签发数据,所以卫光生物和上海莱士批签发数存在增加可能。截止2026.1.18日各检验所公布数据,上海莱士2025年以108批签发次稳居榜首,遥遥领先。此外,上海莱士2024年和2025年还各有18批次的人纤维蛋白粘合剂。
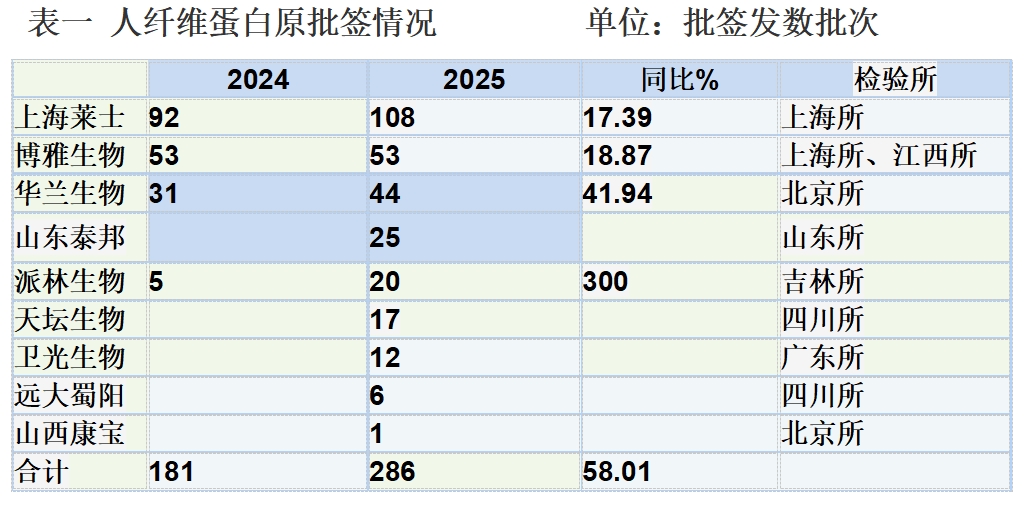 由于人纤维蛋白原毛利率高,而且根据有关研究机构研报数据显示,预计全球人纤维蛋白原将以15.5%的年复合增长率(CAGR)持续扩张至2031年,市场规模将从2024年的10.59亿美元增长到28.66亿美元,因此各血制品生产企业均在加快人纤维蛋白原的研发生产力度,2025年国内山东泰邦、天坛生物、卫光生物、远大蜀阳和山西宝康人血纤维蛋白都开始生产上市。派林生物2024年四季度开始生产,按季度平均数来看,2025年增幅不明显,可能与广东双林和派斯菲科技改影响有关。
由于人纤维蛋白原毛利率高,而且根据有关研究机构研报数据显示,预计全球人纤维蛋白原将以15.5%的年复合增长率(CAGR)持续扩张至2031年,市场规模将从2024年的10.59亿美元增长到28.66亿美元,因此各血制品生产企业均在加快人纤维蛋白原的研发生产力度,2025年国内山东泰邦、天坛生物、卫光生物、远大蜀阳和山西宝康人血纤维蛋白都开始生产上市。派林生物2024年四季度开始生产,按季度平均数来看,2025年增幅不明显,可能与广东双林和派斯菲科技改影响有关。
此外,根据血制品上市公司2024年年报、2025年半年报和公司公告整理,有4家血制品公司控股子公司均在研发人纤维蛋白原:2025年10月1日天坛生物发布公告,公司下属企业国药集团昆明血液制品有限公司获得国家药品监督管理局签发的《药物临床试验批准通知书》,同意开展“人纤维蛋白原”临床试验;华兰生物2024年年度报告载明公司子公司华兰生物工程重庆有限公司已开展人纤维蛋白原临床前研究;上海莱士2025年2月13日公告郑州莱士血液制品有限公司收到国药监局下发的关于“人纤维蛋白原”药物临床试验批准通知书;2023年4月29日派林生物发布了《关于子公司收到人纤维蛋白原临床试验数据核查与注册现场核查通知的公告》,广东双林生物制药有限公司收到国家药品监督管理局药品审评中心的《药审中心关于启动人纤维蛋白原临床试验数据核查的通知》和《药审中心关于启动人纤维蛋白原注册现场核查的通知》,药审中心根据《药品注册管理办法》有关规定,对广东双林申报注册的人纤维蛋白原(受理号:CXSS2300008)启动药品注册核查(临床)和药品注册核查(药学)(这么久了为何没有下文,公司财报中一字未提)。
随着各大公司人纤维蛋白原的陆续投产,未来竞争日趋激烈在所难免,血浆采集量是公司确保竞争地位的基础。
附 血制品公司人纤维蛋白原2024、2025批签发号