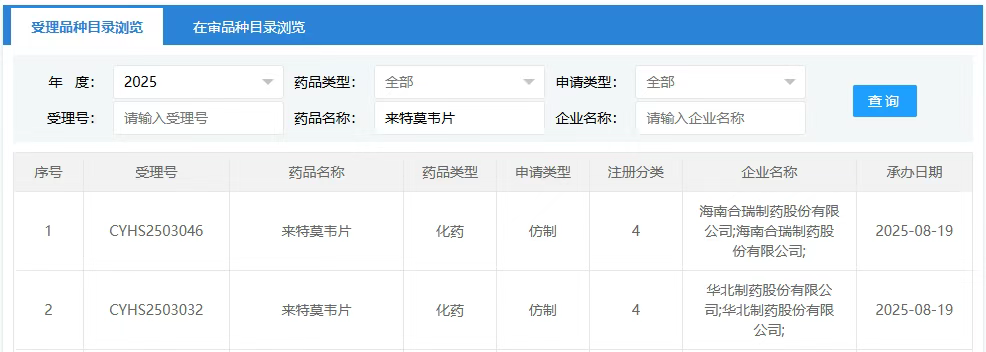
8月19日,CDE官网显示,海南合瑞制药和华北制药递交了4类仿制化药来特莫韦片的上市申请,均获受理。据摩熵医药数据库信息,来特莫韦2024年全球销售额约8亿美元,该剂型国产第三家的席位正在激烈争夺中。
来特莫韦(Letermovir)是一种新型非核苷巨细胞病毒抑制剂,主要用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病。
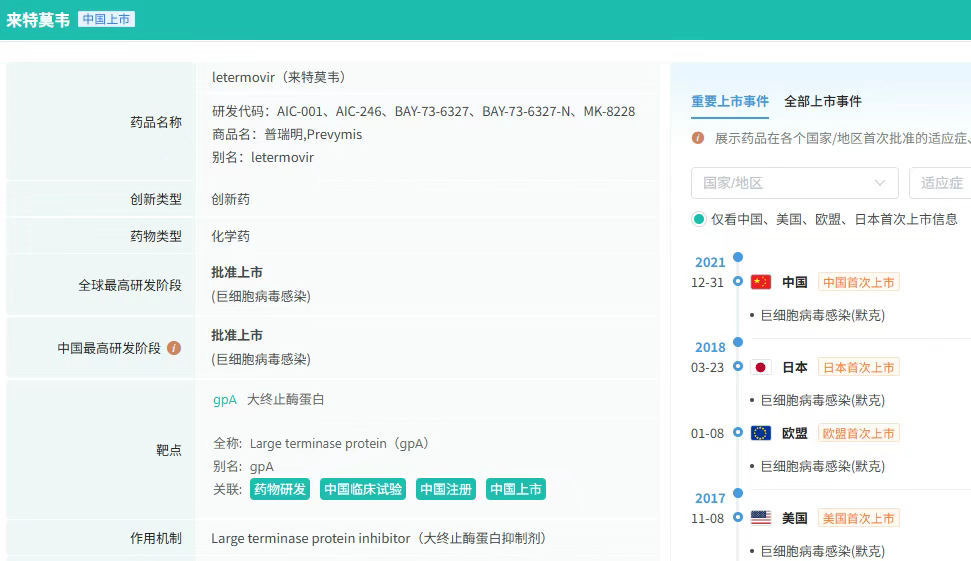
该药物的原研权益由默沙东通过旗下子公司从AiCuris公司收购获得。来特莫韦片剂和注射剂最早于2017年获美国FDA批准上市,2022年先后获批进入国内市场,商品名为Prevymis(普瑞明)。
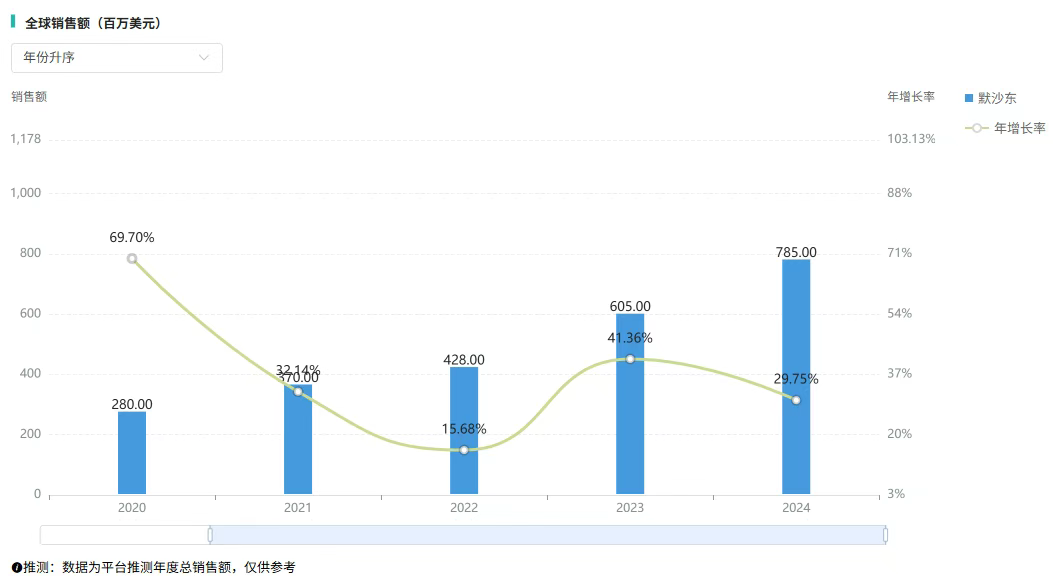
近年来,来特莫韦的全球销售额保持快速增长态势,2023年突破6亿美元,2024年同比递增29.75%,达7.85亿美元。
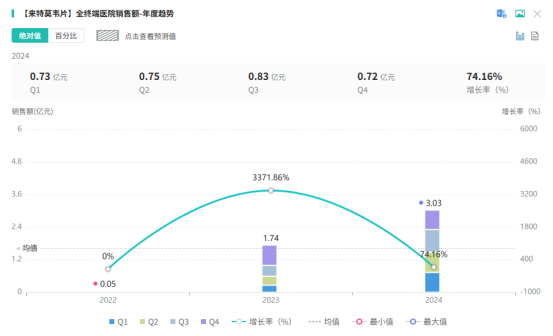
在全国院内市场,来特莫韦片表现同样抢眼,2022年院内销售额为500多万元,2023年跃升至1.74亿,同比增幅高达3371.86%;2024年销售额近乎翻倍,达3.03亿,同比增长74.16%。
巨细胞病毒(CMV)又被称为人类巨细胞病毒,是最大的人类疱疹病毒。其以隐性感染为主,能引发较高的死亡率及严重疾病。我国巨细胞病毒感分布广泛,普通人群CMV抗体阳性率为86%-96%,孕妇约为95%,婴幼儿期为60%-80%。原发感染多发生于婴幼儿时期,一旦感染,将持续终身。
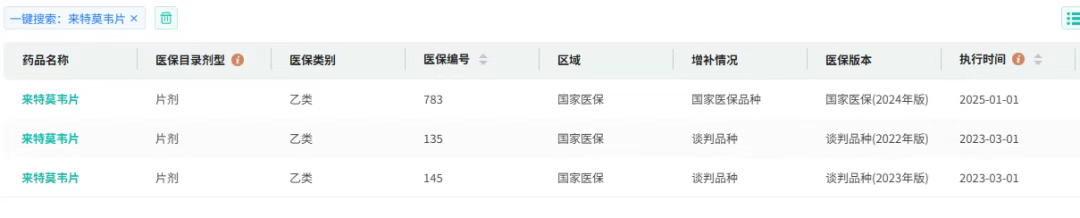
2023年,来特莫韦片/注射液通过国谈被纳入国家医保乙类药物目录。目前来特莫韦片单盒销售价格(规格:240mg*28片/盒)仍超过4000元,市场潜力十分可观。
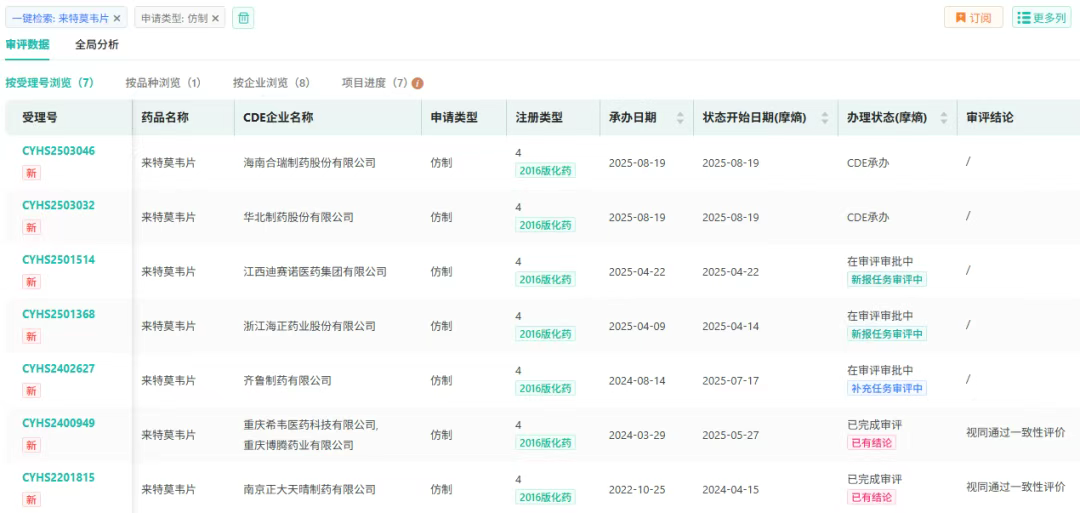
从仿制竞争格局来看,2024年4月,正大天晴的来特莫韦片历时近一年半获NMPA批准上市,拿下国内首仿;重庆希韦医药则斩获国产第二家。同年,正大天晴再下一城,将来特莫韦注射液的首仿资格收入囊中。

目前,除前文提及的海南合瑞制药与华北制药外,齐鲁制药、浙江正海医药、江西迪赛诺医药这3家企业也在进行来特莫韦片的上市申请。
此外,原研企业默沙东(MSD)于今年3月向CDE提交了来特莫韦微片这一新剂型的进口上市申请,该申请已被纳入优先审评程序,预计今年年末有望获批。据CDE公示信息,来特莫韦微片属于儿童专用新品种,这一剂型的补充将为患者提供更多用药选择。

来特莫韦的化合物专利在中国的保护期已于2024年4月届满,随着多家企业的积极布局,其市场即将迎来更为激烈的竞争。

而仿制药竞争的加剧与新剂型的推出,将推动来特莫韦进一步普及,为我国巨细胞病毒感染患者提供更易获取、更经济的治疗选择,从而更好的满足临床需求。

